キャピラリー電気泳動装置・方法
キャピラリー電気泳動における分離の原理
キャピラリー電気泳動における試料分離の原理は、寒天を用いた電気泳動の原理とは異なります。
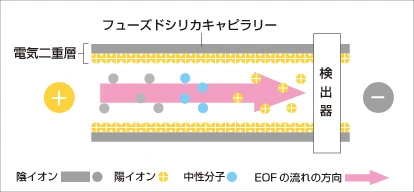
キャピラリー電気泳動では、物質の「イオン半径の大きさ」と「電荷の大きさ」の違いによって分離が進行します。試料に含まれる個々の物質は、緩衝液の液性の影響下においては、プラスやマイナスの電荷を帯びるか、またはそのどちらでもない中性の状態をとります。その状態の試料に電圧をかけると、物質は自らが持つ電荷とは反対の電極へ移動します。その移動速度は物質の半径が小さいほど、電荷の強さが強いほどに早くなり、泳動中の試料は徐々に分離が進行していきます。
また、電気泳動で使用されるキャピラリーはフューズドシリカ製で、電気泳動の際、この管の内壁を取り巻くシラノール基(≡Si-OH)の影響によって「電気浸透流(EOF)」と呼ばれる緩衝液の流れがキャピラリーの管の中に発生します。この電気浸透流は電荷による試料の移動速度より1桁ほど早い緩衝液の流れを発生させます。そのため、キャピラリー電気泳動では、一度の分析で陽イオン・陰イオン・中性分子(非イオン性化合物)の全ての検出が可能となるのです。
キャピラリー電気泳動装置の実用動向
無機イオン(Mg2+、Na+、PO43-、NH4+、・・・)、有機イオン(有機酸、アミノ酸、糖・・・)等の中・低分子から、タンパク質・糖鎖・DNA・RNAの生体高分子まで、幅広い分析に使用されます。
これら幅広い分析対象範囲は、様々な分離モードが開発されてきたことで可能となっています。
- キャピラリーゾーン電気泳動(CZE)
- 最も一般的な分離方法で無機イオン類、有機イオン類等を分離させる方法
- ミセル導電クロマトグラフィー(MEKC)
-
キャピラリー電気泳動(CE)とクロマトグラフィーの原理を組み合わせた分離分析法。電気的性質を有さない中性分子の分離が容易にできる。
緩衝液に界面活性剤であるSDSを添加し、負に荷電したミセルを形成させ、これに中性分子を取り込ませて分離させる。電気泳動ではあるが、移動相と固定相のあいだの分配係数の差異に基づいて分離するため、このような名称が使われている。 - キャピラリーゲル電気泳動(CGE)
- DNAシーケンシングで使用される方法。ゲルを形成する網目構造による分子ふるい効果を利用し、電気浸透流を抑えた泳動分離方法で、DNA以外にタンパク質等の生体高分子の分離に用いられている。
- キャピラリー等電点電気泳動(cIEF)
-
キャピラリー内にpH勾配を作り出し、タンパク質を等電点で分離する方法。 また、GCやHPLCと同様に質量分析装置と連結させた装置は、より高度な研究(プロテオーム解析、メタボローム解析)に対して使用実績を持つ。
さらに、これまでのDNA塩基配列の決定に寄与してきた実績や、医薬品・化学・食品関連会社等の幅広い領域で使用されており、有用な分離分析装置として認知されている。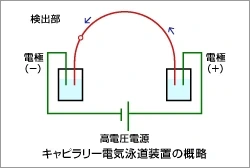
電気浸透流(Electro Osmotic Flow:EOF)
電気浸透流(EOF)とはキャピラリー電気泳動特有の現象で、電気泳動中に陽極から陰極に向けて緩衝液の移動が起こる現象を言います。
この現象は、キャピラリー内壁を取り巻くシラノール基(≡Si-OH)が充填された緩衝液の影響で(≡Si-O-)に解離・帯電することで起きます。解離・帯電した内壁には、緩衝液に含まれる陽イオンが集まり、電気二重層が形成されます。電圧をその状態のキャピラリーに印可すると、結合していた陽イオンが一斉に陰極に移動するため、緩衝液に陰極への流れを生み出します。